

Protective effect of the long pentraxin PTX3 against histone-mediated endothelial cell cytotoxicity in sepsis
Daigo K, Nakakido M, Ohashi R, Fukuda R, Matsubara K, Minami T, Yamaguchi N, Inoue K, Jiang S, Naito M, Tsumoto K, Hamakubo T.
Sci. Signal., 16 September 2014; Vol. 7, Issue 343, p. ra88
ペントラキシン3(PTX3)は液性パターン認識受容体(Soluble pattern recognition receptor)として自然免疫反応に重要な役割を担う分泌タンパクです。またCRP(C-reactive protein)、SAP(Serum amyloid P component)などの急性期タンパクの一つでもあります。CRP、SAP、PTX3はカルボキシル基末端側にペントラキシンドメインを有するペントラキシンファミリーに属しています。更にPTX3は比較的長いアミノ基末端領域を有している事からロングペントラキシン(long pentraxin)に分類されます。PTX3は真菌、緑膿菌、ウイルスなどを認識し、補体系およびオプソニン化を介して除去する機能を有しています。
敗血症においてPTX3は血中濃度が通常濃度の約100倍にまで上昇します。敗血症においてPTX3は複数の防御機構を有していることは知られていましたが、その詳細は不明なままでした。我々は敗血症におけるPTX3の新たな役割を探るため、PTX3結合タンパクの同定を試み、その中で細胞外ヒストンを見出したことを以前報告しています。細胞外ヒストンは敗血症患者血中に出現し、血管内皮細胞への障害性をきたすことで敗血症死亡の主要因となることが最近になって明らかになってきました。以上のことから、今回我々はヒストンとPTX3の結合メカニズムと、それがヒストンの障害性にどのような影響を及ぼすかをより詳細に解析し報告しました。
一般的なタンパク結合の解析手法から、ヒストンとPTX3は通常のタンパク質相互作用としては非常に強い結合性を示しました。そこで東京大学工学系研究科の津本浩平教授らと共同でより詳細に解析した結果、本結合はタンパク質の構造が失われる凝集反応であることが明らかになりました(図1)。
さらに培養ヒト血管内皮細胞を用いてPTX3がヒストンによる内皮細胞障害を抑制することを見出しました。興味深いことに、ヒストンとの凝集性、ヒストンによる内皮細胞障害性の抑制性どちらについてもPTX3のアミノ基末端領域が十分な領域であることが示されました。そこでPTX3アミノ基末端領域の投与が敗血症に有効かどうかマウスを用いた実験で確認しました。マウスにヒストンを投与すると肺出血を起こして死亡することが知られていますが、PTX3の投与で血管内皮細胞の障害と肺出血が抑制され、生存率が改善されました(図2)。また敗血症モデルマウスにおいてもPTX3の投与で炎症反応が抑制され、生存率が改善されました。
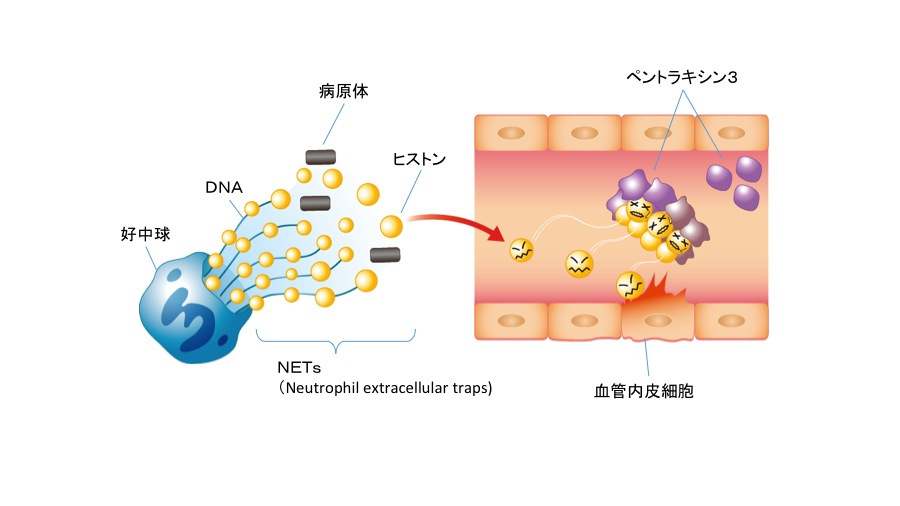
以上の結果はPTX3の新たな自然免疫機構の発見であるとともに、敗血症や細胞外ヒストンによる疾患に対する治療方策を提供するものとして期待されます(図3)。
本研究は東京大学大学院工学系研究科バイオエンジニアリング専攻の津本浩平教授研究グループ、新潟大学大学院医歯学総合研究科細胞機能講座分子細胞病理学分野の内藤眞教授研究グループおよび新潟大学医歯学総合病院病理部の大橋瑠子特任助教、順天堂大学医学部練馬病院循環器内科の井上健司准教授研究グループとの共同研究です。